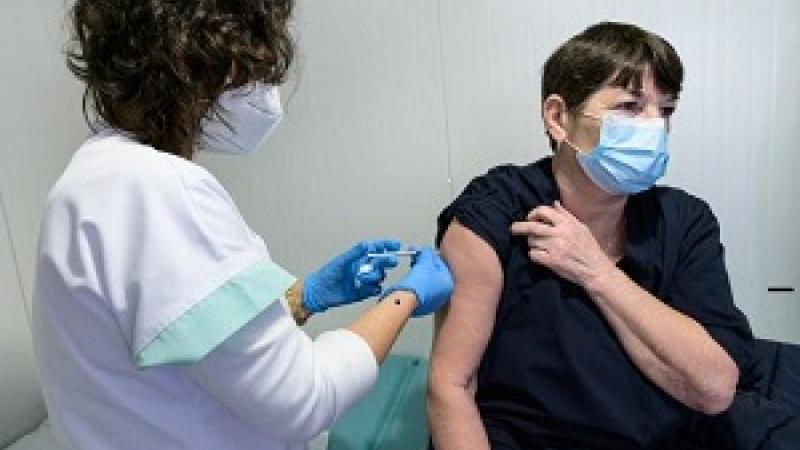
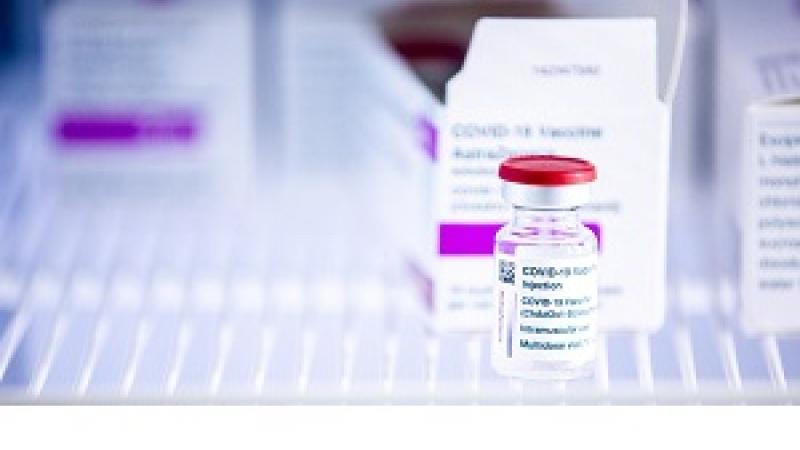
Agencia Europea del Medicamento
Los reguladores globales discuten el camino hacia la alineación regulatoria en respuesta a la variante de Omicron
El 12 de enero, los reguladores de todo el mundo discutieron la respuesta regulatoria global a la variante COVID-19 Omicron durante un taller, copresidido por la Agencia Europea de Medicamentos (EMA) y la Administración de Alimentos y Medicamentos de EE. UU. (FDA) bajo el paraguas de la Coalición Internacional de Autoridades Reguladoras de Medicamentos (ICMRA). El objetivo de la reunión fue revisar la evidencia disponible sobre la efectividad de las vacunas COVID-19 aprobadas contra la variante de Omicron y lograr la alineación con los requisitos regulatorios clave para respaldar el desarrollo de una posible vacuna adaptada.
Dando la bienvenida a los participantes de los 24 miembros y 13 miembros asociados y expertos de la Organización Mundial de la Salud (OMS) y la Comisión Europea, Emer Cooke, directora ejecutiva de EMA y presidenta de ICMRA, dijo: "Hoy no se trata solo de la respuesta regulatoria a Omicron, sino también es parte de preparar el escenario para una discusión más estratégica sobre qué tipos de vacunas podrían ser necesarias a largo plazo para manejar adecuadamente el COVID-19. Estas decisiones no son solo para los reguladores. Se necesita la colaboración de todos los actores en este espacio, incluidos los responsables de la toma de decisiones en materia de salud pública a nivel nacional, regional y mundial. En ese contexto, debemos enfatizar la importancia de la colaboración con la OMS para tomar una decisión sobre las actualizaciones de cepas”.
Si bien la mayoría de los datos disponibles sugieren que las vacunas COVID-19 aprobadas están perdiendo efectividad en la protección contra infecciones y enfermedades leves, continúan brindando una alta protección contra las personas que desarrollan enfermedades graves y la necesidad de hospitalización relacionada con la variante Omicron.
Fuente: EMA