Agencia Europea del Medicamento
La EMA recomienda la autorización de Nuvaxovid en la UE
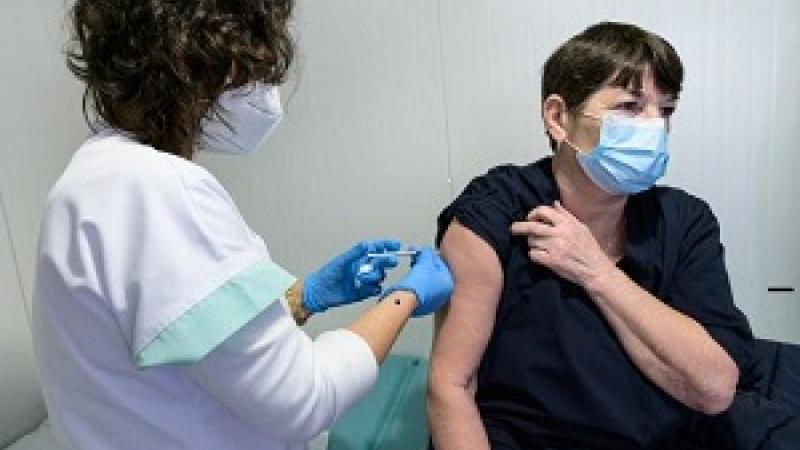
La EMA ha recomendado otorgar una autorización de comercialización condicional para la vacuna COVID-19 Nuvaxovid de Novavax (también conocida como NVX-CoV2373) para prevenir la COVID-19 en personas a partir de los 18 años.
Nuvaxovid es la quinta vacuna recomendada en la UE para prevenir COVID-19. Es una vacuna a base de proteínas y, junto con las vacunas ya autorizadas, apoyará las campañas de vacunación en los Estados miembros de la UE durante una fase crucial de la pandemia.
Después de una evaluación exhaustiva, el comité de medicamentos humanos (CHMP) de la EMA concluyó por consenso que los datos sobre la vacuna eran sólidos y cumplían los criterios de la UE en cuanto a eficacia, seguridad y calidad.
Los resultados de dos ensayos clínicos principales encontraron que Nuvaxovid fue eficaz para prevenir el COVID-19 en personas a partir de los 18 años. Los estudios involucraron a más de 45.000 personas en total. En el primer estudio, alrededor de dos tercios de los participantes recibieron la vacuna y los demás recibieron una inyección de placebo (ficticia); en el otro estudio, los participantes se dividieron por igual entre Nuvaxovid y placebo. Las personas no sabían si habían recibido Nuvaxovid o un placebo.
Fuente: EMA