Agencia Europea del Medicamento
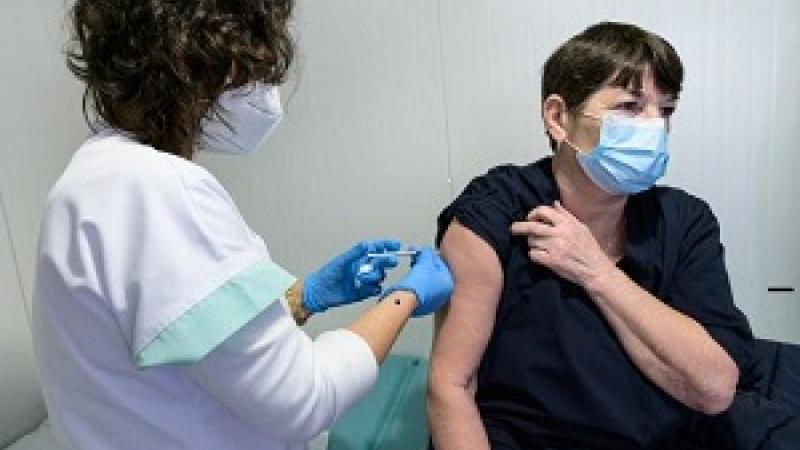
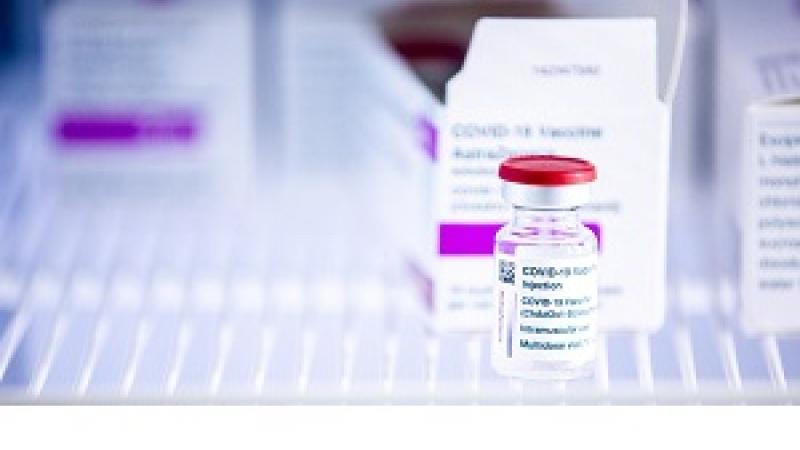
La EMA recibe la solicitud de autorización de comercialización condicional de la vacuna COVID-19 de Novavax, Nuvaxovid
La EMA ha comenzado a evaluar una solicitud de autorización de comercialización condicional para la vacuna COVID-19 de Novavax, Nuvaxovid (también conocida como NVX-CoV2373). La evaluación se llevará a cabo con un cronograma acelerado, y se podría emitir una opinión sobre la autorización de comercialización en unas semanas si los datos presentados son lo suficientemente sólidos y completos para demostrar la eficacia, seguridad y calidad de la vacuna.
Un período de tiempo tan corto solo es posible porque la EMA ya ha revisado una parte sustancial de los datos sobre la vacuna durante una revisión continua. Durante esta fase, el comité de medicamentos humanos (CHMP) de la EMA evaluó datos de estudios de laboratorio (datos no clínicos), cierta información sobre la calidad de la vacuna y la forma en que se producirá, y datos sobre su seguridad, inmunogenicidad (qué tan bien desencadena una respuesta frente al virus) y eficacia frente a COVID-19 de estudios clínicos en adultos.
Paralelamente, el comité de seguridad de la EMA (PRAC) completó la evaluación preliminar del plan de gestión de riesgos (PGR) propuesto por la empresa, que describe las medidas para identificar, caracterizar y minimizar los riesgos del medicamento.
Fuente: EMA