Agencia Europea del Medicamento
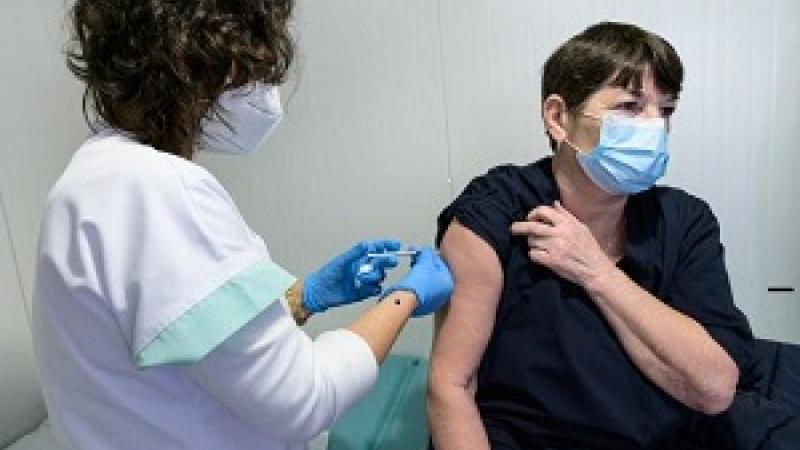
La EMA comienza a evaluar el uso de la vacuna COVID-19 Spikevax en niños de 6 a 11 años
La Agencia Europea del Medicamento ha comenzado a evaluar una aplicación para extender el uso de la vacuna COVID-19 de Moderna, Spikevax, a niños de 6 a 11 años.
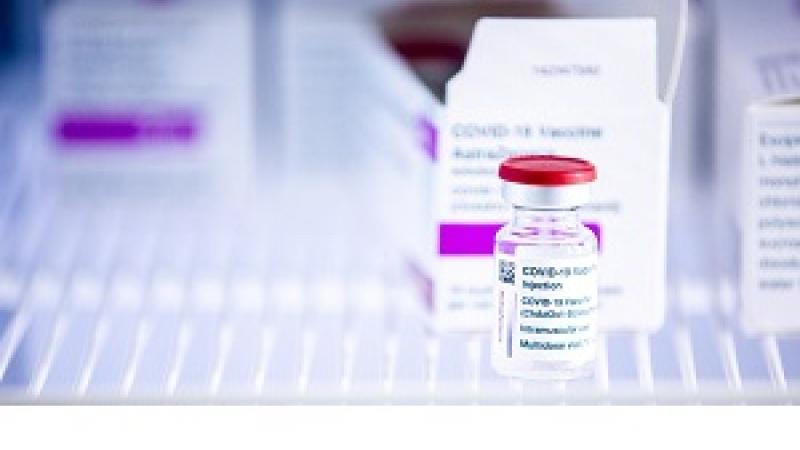
Spikevax es una vacuna para prevenir COVID-19, actualmente autorizada para su uso en personas de 12 años o más. Contiene una molécula llamada ARN mensajero (ARNm) con instrucciones para producir una proteína, conocida como proteína de pico, que está presente de forma natural en el SARS-CoV-2, el virus que causa el COVID-19. La vacuna actúa preparando al cuerpo para defenderse del SARS-CoV-2.
El comité de medicamentos humanos (CHMP) de la EMA revisará los datos sobre la vacuna, incluidos los resultados de un estudio clínico en curso con niños de 6 a 11 años, para decidir si recomendar extender su uso. El cronograma de cualquier evaluación siempre depende de los datos que se envían. El cronograma actual para la evaluación prevé una opinión en aproximadamente 2 meses, a menos que se necesite información o análisis complementarios. Este es un calendario más corto en comparación con tipos similares de revisiones fuera de una pandemia.
La Agencia comunicará el resultado de su evaluación. A continuación, la opinión del CHMP se enviará a la Comisión Europea, que emitirá una decisión final.
Fuente: EMA