Agencia Europea del Medicamento
Vacuna COVID-19 Spikevax aprobada para niños de 12 a 17 años en la UE
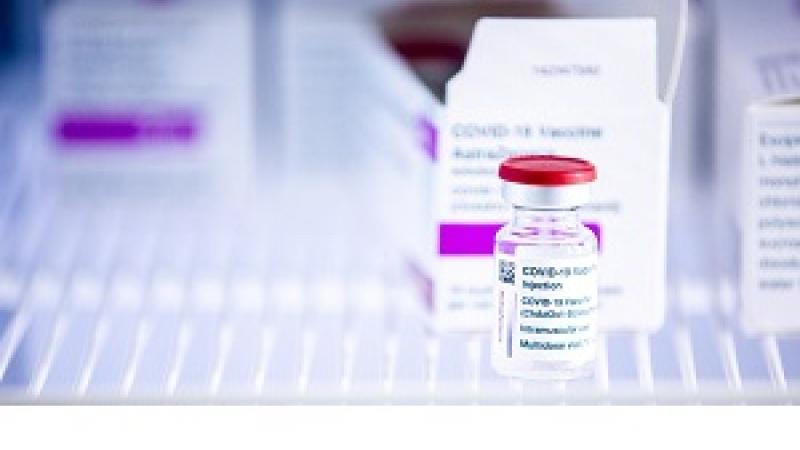
El comité de medicamentos humanos de la EMA (CHMP) ha recomendado otorgar una extensión de la indicación para la vacuna COVID-19 Spikevax (anteriormente COVID-19 Vaccine Moderna) para incluir el uso en niños de 12 a 17 años. La vacuna ya está autorizada para su uso en personas mayores de 18 años.
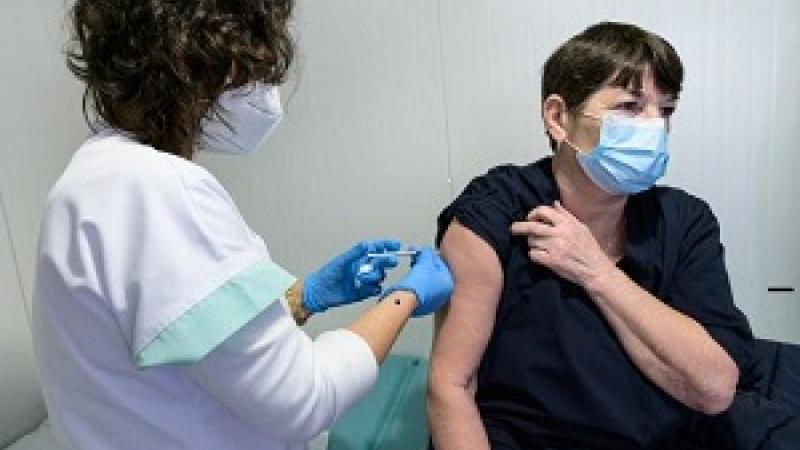
El uso de la vacuna Spikevax en niños de 12 a 17 años será el mismo que en personas mayores de 18 años. Se administra en dos inyecciones en los músculos de la parte superior del brazo, con cuatro semanas de diferencia.
Los efectos de Spikevax se han investigado en un estudio en el que participaron 3.732 niños de entre 12 y 17 años. Este estudio en curso se está llevando a cabo de acuerdo con el plan de investigación pediátrica (PIP) de Spikevax, que fue acordado por el Comité Pediátrico de la EMA (PDCO).
El estudio mostró que Spikevax produjo una respuesta de anticuerpos comparable en jóvenes de 12 a 17 años a la observada en adultos jóvenes de 18 a 25 años (medida por el nivel de anticuerpos contra el SARS-CoV-2). Además, ninguno de los 2.163 niños que recibieron la vacuna desarrolló COVID-19 en comparación con cuatro de los 1.073 niños que recibieron una inyección ficticia. Estos resultados permitieron al CHMP concluir que la eficacia de Spikevax en jóvenes de 12 a 17 años es similar a la de los adultos.
Fuente: EMA